Bu ders notumuzda Kimya dersinin Kimyasal Hesaplamalar konusu altında; Mol Nedir? Avogadro Sayısı, Kimya Kanunları (Kütle Korunumu Kanunu, Sabit Oranlar Kanunu, Katlı Oranlar Kanunu, Atom Ağırlığını Bulma, Denklemli Kimya Problemleri, Artık Madde Problemleri, Karışım Problemleri, Örnek Soru Çözümleri vb. başlıklar hakkında detaylı bilgileri bulabilirsiniz.
KİMYASAL HESAPLAMALAR:
• MOL KAVRAMI
Mol: 6,02.1023 taneciğe 1 mol denir.
Bu sayıya Avogadro sayısı denir.
Bazı işlemlerde kısaltma olarak (No: Avogadro sayısı) gösterilir.
1 mol Mg atomu 6,02.1023 tane atom içerir.
1 mol H2SO3 molekülü 6,02.1023 tane molekül içerir.
1 mol Al2(SO4)3 molekülü 6,02.1023 tane molekül içerir.
1 mol H2 molekülü 6,02.1023 tane molekül içerir.
Bir atomun gram türünden miktarına atom-gram (1 mol atom) denir.
Bir bileşiğin molekül kütlesinin gram türünden miktarına molekül-gram (1 mol molekül) denir.
1 mol H2SO4 bileşiği: H: 1, S: 32, O : 16 olmak üzere 2.1 + 32 + 4.16 = 98 gram olarak bulunur.
Bir iyonun gram türünden miktarına iyon–gram denir.
| Gazlar için; Normal şartlar altında (N.Ş.A.), (0°C, 1 atm) 1 mol gaz, 22,4 lt.dir. |
BİLEŞİK FORMÜLÜ BULMA PROBLEMLERİ
Kaba Formül (Basit Formül)
Bir bileşiği oluşturan atomların cinsini ve oranını belirten formüldür. Kaba formülde molekülü oluşturan atomların kaçar tane olduğu bilinemez.
Gerçek Formül (Molekül Formülü)
Bir bileşiği oluşturan atomların cinsini oranını ve sayısını belirten formüldür. Molekül formülünde simgelerin altındaki sayılar, bileşiğin bir molekülü içindeki element atomlarının gerçek sayılarını gösterir.
| Bir bileşiğin kaba formülünün bulunabilmesi için bileşiği oluşturan atomların ayrı ayrı mol sayıları bulunur ve bu sayılar en küçük tamsayılar haline getirilir. Şayet bileşiğin gerçek (molekül) formülü isteniyorsa kaba formül bulunduktan sonra bileşiğin mol ağırlığı ya da içerdiği toplam atom sayısı verilmelidir. |
KİMYA KANUNLARI
1. Kütle Korunumu Kanunu
Reaksiyona girenlerin kütleleri toplamı, reaksiyondan çıkanların kütleleri toplamına eşittir.
Örnek – 2
Aşağıda bazı maddelerin molekül ağırlıkları verilmiştir.
X in mol ağırlığı : 160 g/mol
Y nin mol ağırlığı : 28 g/mol
Z nin mol ağırlığı : 56 g/mol ise
X + 3Y ® 2Z + 3T
T’nin mol ağırlığı kaçtır?
Çözüm
Verilenler mol ağırlığı ise katsayısı ile çarpılıp ürünler girenlere eşitlenmelidir.

2. Sabit Oranlar Kanunu
Bir bileşiği oluşturan elementlerin ağırlıkları arasında sabit bir oran vardır.
Fe2O3 bileşiğinde (Fe: 56, O: 16)
2.56 = 112 gram Fe’ye karşılık
3.16 = 48 g O vardır.
birleşme oranı en sade şekilde 7 gram Fe’ye karşı 3 gram oksijendir.
Örnek – 3
X2Y3 bileşiğinin birleşme oranı 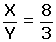 ise hangi sonuçlar çıkarılabilir?
ise hangi sonuçlar çıkarılabilir?
Çözüm
11 gram X2Y3 bileşiğinin 8 gramı X, 3 gramı Y’dir.
Veya: X’in atom ağırlığı 4 ise Y’nin atom ağırlığı 1’dir, sonuçları çıkarılabilir.
3. Katlı Oranlar Kanunu
İki element arasında birden fazla bileşik oluşabiliyorsa, bu bileşiklerde elementlerden birinin sabit miktarına karşı diğerinin değişen miktarı arasında basit ve tam sayılarla ifade edilen orana katlı oranlar denir.
Örnek – 4
NO ve NO2 bileşiklerinde;
| Bileşik | N miktarı | Oksijen Miktarı | 14 gram N ilebirleşen O Miktarı |
| NO | 14 | 16 | 16 |
| NO2 | 14 | 32 | 32 |
görüldüğü gibi her iki bileşikte 14 gram N ile birleşen oksijenlerin kütlelerinin oranı:

ATOM AĞIRLIĞI BULMA PROBLEMLERİ
Bir bileşik içerisinde atom ağırlığı bilinmeyen elementlerin atom ağırlığını bulabilmek için öncelikle bileşiğin 1 molünün ağırlığı bulunmalıdır. Atom ağırlığı verilenler kullanılarak sorulan atom bulunur.
Örnek – 5
9,6 gram oksijen içeren X2O3 bileşiği 32 gram ise X in atom ağırlığı kaçtır? (O : 16)
Çözüm
Önce bileşiğin mol sayısını hesaplayalım.
1 mol X2O3 te 48 gram oksijen varsa
x mol X2O3 9,6 gram oksijen varsa
__________________________________
x = 0,2 mol
0,2 mol X2O3 32 gram ise
1 mol X2O3 x
__________________________________
x = 160 gram
1 mol X2O3 160 gram olduğuna göre
2X + 3.16 = 160
x = 56 olarak bulunur.
DENKLEMLİ KİMYA PROBLEMLERİ
Kimyasal hesaplamaların denklemler yardımıyla yapılmasını bu başlık altında inceleyeceğiz.
Bu tip problemlerde;
- Denklem verilmiş ise denklemin denk olup olmadığı kontrol edilmeli, denklem denk değilse denkleştirilmelidir.
- Hangi maddelerin reaksiyona girip hangi maddelerin oluştuğu verilir. Bunlar denklemde yerine yazılmalı ve denklem denkleştirilmelidir.
- Reaksiyona giren maddeler verilir fakat ürünler belirtilmez. Bu durumda denklem yazılmalıdır ve denkleştirilmelidir.
2Al + 3S ® Al2S3 denklemine göre (Al: 27,S:32);
- 2 mol alüminyum 3 mol S ile reaksiyona girmiş 1 mol Al2S3 oluşmuştur.
- 54 g Alüminyum 96 gram S ile reaksiyona girerse 150 gram Al2S3 oluşturur.
- 2. 6,02.1023 tane Al, 3.6,02.1023 tane S ile tepkimeye girdiğinde 6,02.1023 tane Al2S3 oluşur.
yorumları yapılabilir.
Örnek – 6
9 g Al yeterli miktarda HNO3 ile reaksiyona girerek çözünüyor.
a. Kaç mol HNO3 gerekir?
b. Oluşan H2 gazı normal koşullarda kaç litredir?
Çözüm
Denklem yazılıp eşitlenir.
Al + 3HNO3 ® Al(NO3)3 + 3/2H2
1 mol 3 mol 1 mol 1,5 mol
a. Önce Al nin mol sayısını bulalım 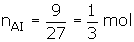
mol Al 3 mol HNO3 ile reaksiyona girerse
 x
x
x = 1 mol HNO3 gerekir.
b. 1 mol Al dan 1,5 mol H2 oluşursa
 x
x
x = 0,5 0,5 0,5 0,5 mol H2(g) oluşur.
VH2 = 0,5 x 22,4 = 11,2 Lt H2 oluşur.
ARTIK MADDE PROBLEMLERİ
Reaksiyona giren maddelerden herhangi birinin başlangıçta alınan miktarının sınırlı olması durumunda diğer maddeler ne kadar fazla olursa olsun reaksiyona giremeyecek, yani madde artışı olacaktır.
Oluşan ürün miktarı ise sınırlı olana yani tamamen harcanana bağlı olacaktır.
Örnek – 7
0,3 mol N2 ile 2 gram H2 gazlarının karışımından birisi bitinceye kadar NH3(g) oluşturuluyor.
Aşağıdaki soruları yanıtlayınız? (N : 14, H : 1)
a. Kaç mol NH3(g) oluşur?
b. Reaksiyondan sonra toplam gaz NŞA da kaç lt gelir?
Çözüm
Reaksiyon denklemi yazılıp eşitlenirse
N2(g) + 3H2(g) ® 2NH3(g)
elde edilir. Soruda N2 ve H2 verildiğinden hangisinin az ya da çok olduğu tespit edilmelidir. H2 nin mol sayısı N2 mol sayısının 3 katı olacakmış. N2 gazı 0,3 mol girerse H2 gazı 0,9 mol reaksiyona girer yani H2 gazının 0,1 molü fazladır. Bu durumda;
| a. | AlınanReaksiyona giren
Sonuç |
: :
: |
N2 + 3H2 ® 2NH30,3 mol 1 mol 00,3 mol 0,9 mol 0,6 mol
Biter 0,1 mol 0,6 mol Artar oluşur. |
| b. | Ortamda | Artan gaz : 0,1 molOluşan gaz : 0,6 mol
Toplam gaz : 0,7 mol |
1 mol N.Ş.A’da 22,4 lt ise
0,7 mol x
x =15,68 lt gelir.
KARIŞIM PROBLEMLERİ
Bir karışımdaki herbir maddenin miktarını tespit etmeye yönelik soru tipleridir. Denklemsiz ya da denklemli olarak karşımıza çıkabilir. Reaksiyonlu sorularda maddelerin verdiği reaksiyonlar bilinmelidir. Soruların çözümünde mol ile işlem yapmakta fayda vardır.
0,7 mol X
Örnek – 8
Eşit kütlede CH4 ve SO2 den oluşan karışım 3,01.1022 tane molekül içermektedir.
Buna göre karışımdaki herbir madde kaçar mol dür?
(H: 1, C: 12, O: 16, S: 32,)
Çözüm
CH4 ve SO2 den oluşan karışımın molekül sayısı 3,01.1022 tane ise mol sayısı 0,05 mol dür.
Karışımdaki gazların kütleleri eşit olduğuna göre mol oranları SO2 için x mol ise
CH4 için 4x mol dür.
Buna göre 0,05 mollük karışımın 0,01 molü SO2‘ye 0,04 molü CH4 e aittir.